近日,浙江大学夏大静/吴一华课题组在Journal of Hazardous Materials上在线发表了题为“Low-dose BPA and its substitute BPS promote ovarian cancer cell stemness via a non-canonical PINK1/p53 mitophagic signaling”的研究论文。该研究首次揭示了环境相关剂量的BPA/BPS暴露可通过激活非经典的PINK1/p53介导的线粒体自噬途径增强卵巢癌细胞干性,进而促进卵巢癌的体内转移。

研究背景
双酚A(BPA)被广泛应用于食品、饮料容器、香烟过滤嘴等多种产品的生产。作为一种外源性雌激素,BPA可能促进包括卵巢和乳腺肿瘤在内的多种雌激素相关肿瘤的进展。学术界前期研究已经证实,BPA可以通过抑制性腺激素的合成和代谢来影响激素的体内浓度。BPA对人类健康可能产生的不良影响逐渐受到业界和民众的重视,因此大量 “无BPA”产品和BPA的替代物(如BPS)开始出现。然而,BPS等BPA替代物的毒性特征在很大程度上是未知的,且无论是BPA还是其替代物在癌症进展中的作用仍存在争议。
研究结果
本研究首先根据2013年至2016年NHANES数据分析了人体内部BPA/BPS暴露水平(NHANES 2013–2014 和2015–2016)。结果显示,近年来人群BPA内暴露浓度呈下降趋势,反之其替代物BPS暴露浓度呈上升趋势。BPA/BPS内暴露均值约10nM,其上限可达到200nM。随后我们用0-1000 nM BPA/BPS处理人卵巢癌细胞,发现BPA/BPS处理显著增加了癌症干细胞(CSCs)标记物的表达(OCT4、NANOG和SOX2),上述效应在100 nM已十分显著,符合人体真实BPA/BPS内暴露浓度。
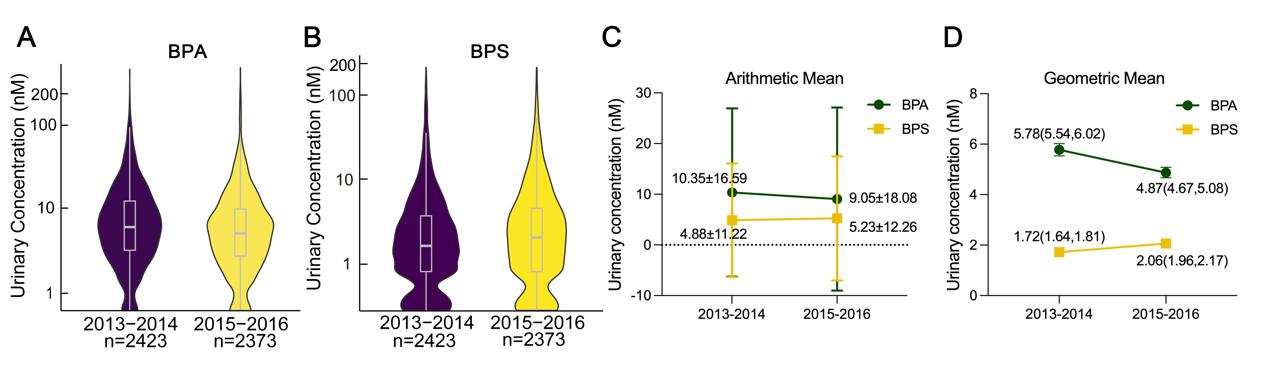
图1 NHANES 2013–2016分析人群BPA/BPS内暴露浓度
进一步的机制研究发现,BPA/BPS暴露所导致卵巢癌细胞干性增强与PINK1介导的线粒体自噬激活密不可分。我们使用课题组自建的ATdb数据库筛选与卵巢癌患者预后不良相关的线粒体自噬相关蛋白,发现PINK1的高表达与卵巢癌患者不良预后高度相关,生存分析同样证实PINK1表达水平较高的卵巢癌患者预后较差。与经典PINK1/Parkin介导的线粒体自噬途径不同,由于Parkin在卵巢癌组织及细胞中表达量极低,因此本研究未继续探究其效应。课题组进一步通过数据分析结合免疫共沉淀及基因突变特征图谱分析发现,PINK1可与p53蛋白互作并参与线粒体自噬的调控。PINK1的激活可促进下游p-p53降解抑制其核转位,从而增强卵巢癌细胞干性。敲低PINK1或线粒体自噬抑制剂Mdivi-1处理,均可显著逆转BPA/BPS诱导的肿瘤细胞干性增强。
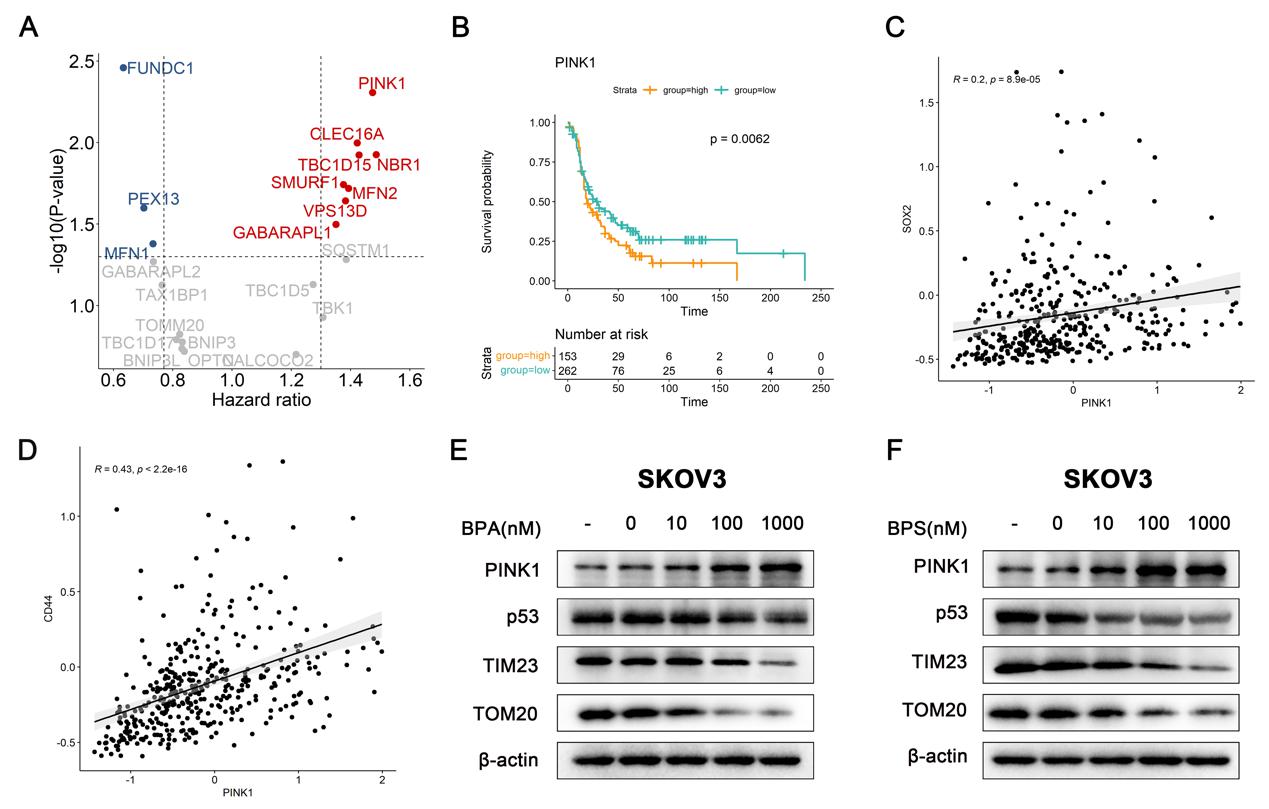
图2 BPA/BPS暴露激活PINK1介导的线粒体自噬途径
进一步的体内研究证实,与对照组相比,暴露于BPA/BPS的小鼠具有更多的肿瘤转移灶,而抑制线粒体自噬有效的阻断了上述效应。免疫组化结果进一步证实CSCs标记物如SOX2等在BPA/BPS暴露组的肿瘤组织中高表达。
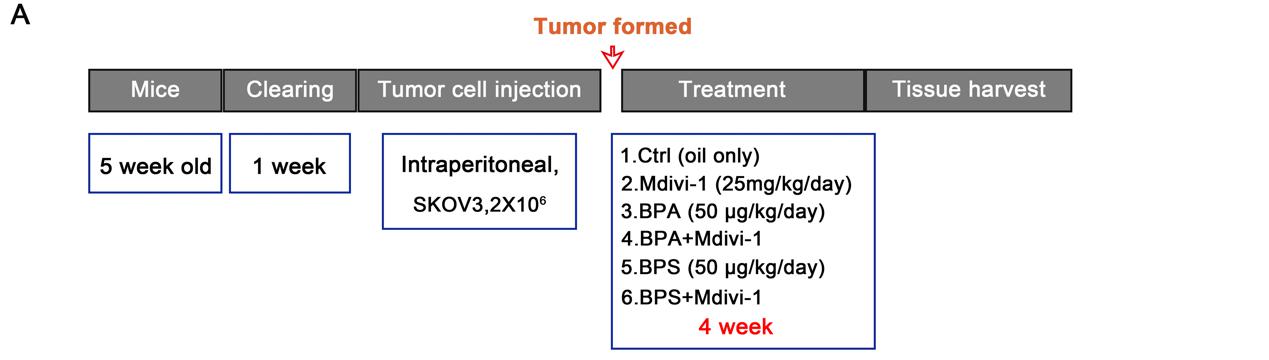
图3 动物体内试验流程图
综上所述,课题组的研究结果创新性揭示了环境相关的BPA/BPS暴露可通过激活非经典的PINK1/p53介导的线粒体自噬途径增强卵巢癌细胞干性,进而促进卵巢癌的体内转移。提示所谓安全的双酚类物质“替代物”是否真正安全仍有待商榷,也为双酚类物质的毒理学评价和风险评估提供了新的依据。
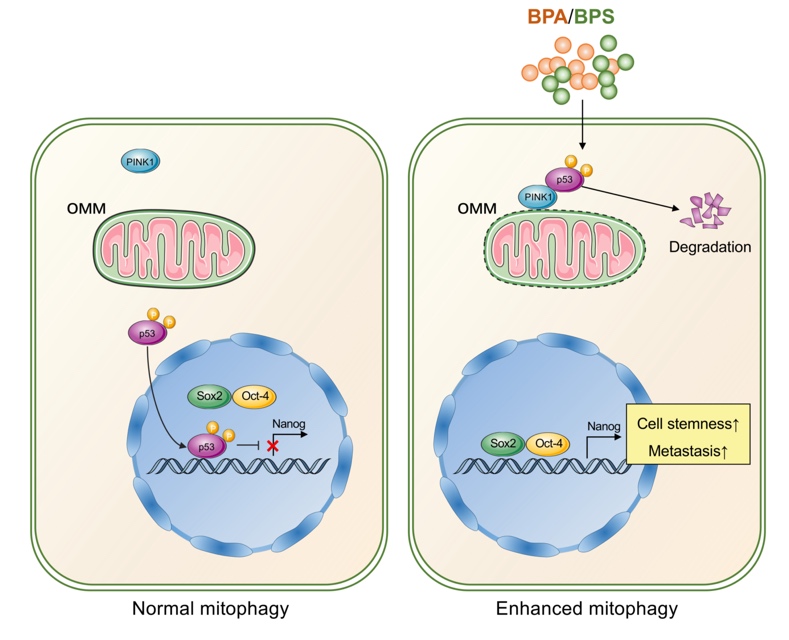
图4 论文摘要图
浙江大学公共卫生学院、附属妇产科医院吴一华副教授和夏大静教授为本文的通讯作者,浙江大学公共卫生学院和附属妇产科医院为共同第一完成单位。公共卫生学院2021级卫生毒理学博士生袁晓宇、附属妇产科医院陈柯列博士后为本文共同第一作者。本课题得到澳门大学沈汉明教授的大力支持和帮助,受到国家自然科学基金、浙江省自然科学基金等资助,并得到浙江大学医学院公共技术平台和实验动物中心的支持。
原文链接:https://doi.org/10.1016/j.jhazmat.2023.13128


